 Anvisa divulga íntegra de documentos que definiram aprovação da vacina para crianças
23 de dezembro de 2021 - 16:40
Anvisa divulga íntegra de documentos que definiram aprovação da vacina para crianças
23 de dezembro de 2021 - 16:40
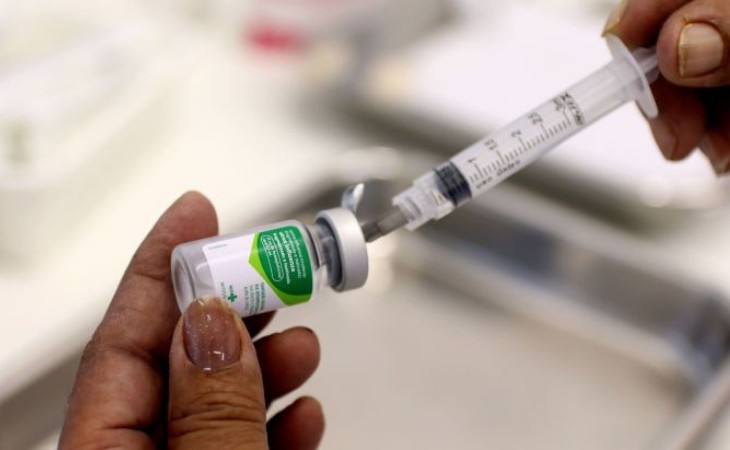
(Foto: Divulgação)
A Agência Nacional de Vigilância Sanitária (Anvisa) divulgou, na última quarta-feira (22), os documentos na integra que definiram a autorização da aplicação da vacina da Pfizer contra a Covid-19 em crianças de 5 a 11 anos de idade no Brasil.
São dois documentos, o parecer público de avaliação de medicamentos (PPAM) e o Parecer Técnico PGR (plano de gerenciamento de riscos). A publicação dos pareceres está alinhada com os princípios da transparência da agência, diz a Anvisa.
De acordo com a Anvisa, o parecer público de avaliação de medicamentos reflete a avaliação de benefício-risco realizada a partir das informações técnicas consideradas pelos técnicos da agência para a aprovação.
Já o Parecer Técnico PGR considera a avaliação da Anvisa sobre o plano de gerenciamento de riscos e reúne as ações de farmacovigilância referentes a ampliação de uso da vacina da Pfizer.
A farmacovigilância compreende a detecção, avaliação, compreensão e prevenção de efeitos adversos ou quaisquer outros possíveis problemas relacionados a medicamentos e imunizantes.
Relacionados